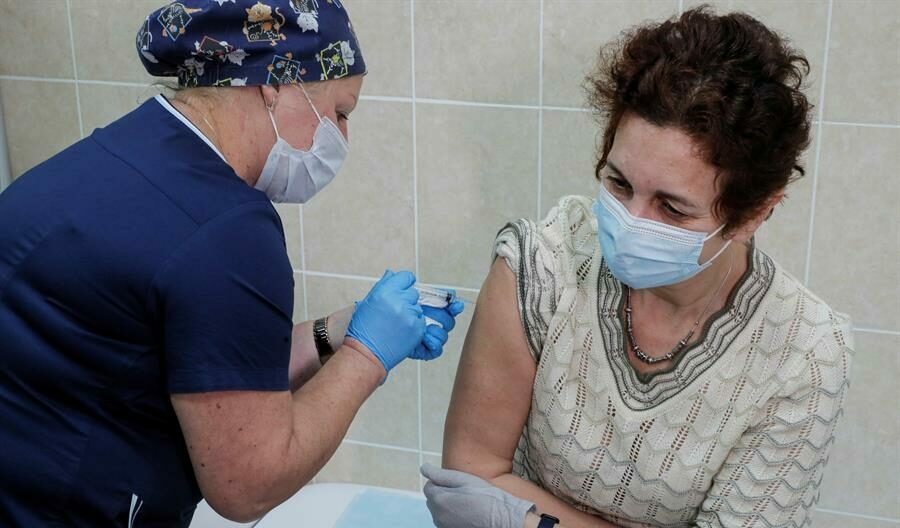
Vacina emergencial terá termo de consentimento do paciente
Anvisa divulgou um guia de orientações para a liberação de imunizantes sem registro
Thamirys Andrade - 03/12/2020 16h00 | atualizado em 03/12/2020 16h03
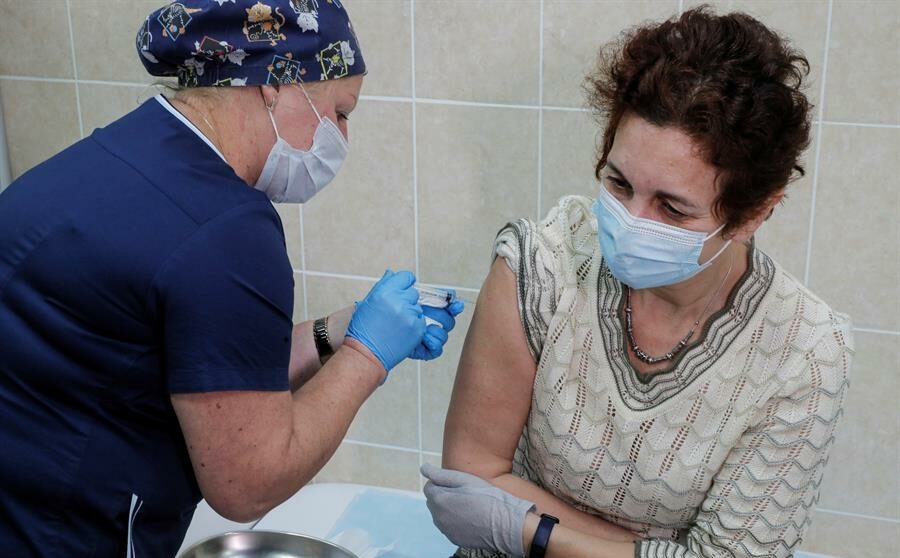
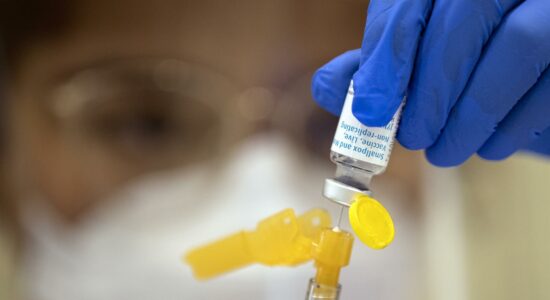
A Agência Nacional de Vigilância Sanitária (Anvisa) divulgou um guia sobre os requisitos necessários para as empresas solicitarem a liberação emergencial de vacinas sem registro. Os imunizantes serão administrados em um grupo pré-definido, que deverá assinar um termo de consentimento, reconhecendo os riscos. No rótulo das vacinas deve constar que se trata de uma vacina experimental.
O guia de orientações para pedidos de liberação provisória vale apenas até o dia 31 de dezembro. Entre os requisitos estão que as empresas fabricantes já devem possuir autorização da Anvisa para produzir e importar medicamentos; os ensaios clínicos devem ter sido realizados no Brasil; o dossiê de desenvolvimento clínico já deve ter passado pelo filtro da agência, assim como os dados sobre a segurança e a eficácia da vacina.
A empresa deve apresentar ainda um relatório sobre a relação risco-benefício do uso emergencial da substância e um plano de monitoramento para detecção de eventos adversos tardios. As desenvolvedoras precisam também se comprometer a concluir as pesquisas e solicitar os devidos registros.
– A autorização de uso emergencial não implica, de nenhuma maneira, em diminuição dos critérios e do rigor de qualidade, segurança e eficácia necessários. Ainda existem dados a serem gerados, ainda existem informações a serem compiladas. Mas se o risco/benefício está bem estabelecido, é possível que concedamos autorização para uso em caráter de emergência – afirmou o gerente-geral de medicamentos da Anvisa, Gustavo Mendes.
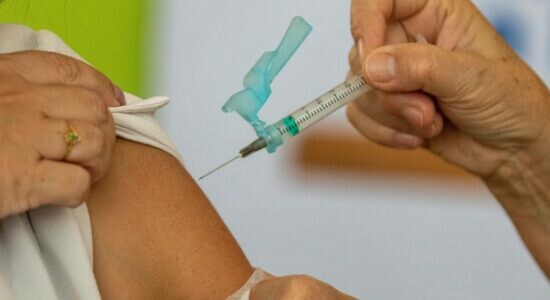
A comercialização das vacinas experimentais não será autorizada, e apenas o Sistema Único de Saúde (SUS) poderá administrar as aplicações. As análises dos pedidos de liberação serão analisados caso a caso e a autorização será temporária, podendo ser revogada a qualquer momento.