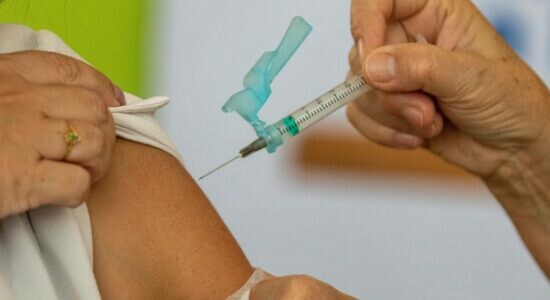
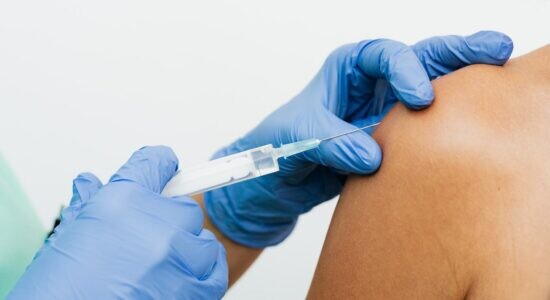
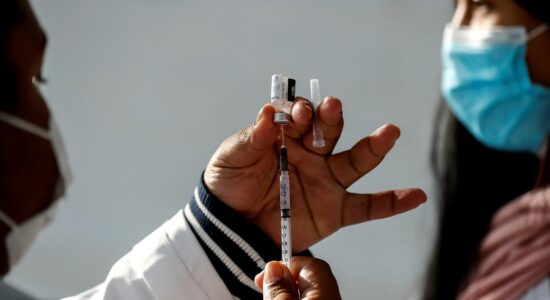
Pfizer volta atrás e avalia uso emergencial de vacina no Brasil
Farmacêutica havia dito que não iria entrar com pedido emergencial na Anvisa
Pleno.News - 30/12/2020 17h00 | atualizado em 30/12/2020 17h26

Após reunir-se com dirigentes e técnicos da Agência Nacional de Vigilância Sanitária (Anvisa) nesta quarta-feira (30), a farmacêutica Pfizer mudou de posição e afirmou que voltou avaliar se pede autorização para uso emergencial de sua vacina contra a Covid-19 no Brasil.
– Uma nova reunião técnica será realizada, e, com base nessa discussão adicional e no andamento das negociações com o governo brasileiro, a Pfizer irá avaliar a possibilidade de solicitar o uso emergencial [da vacina] – declarou a Pfizer em nota.
A autorização para uso emergencial dessa vacina permite o começo da imunização pelo SUS, mas de um público restrito, como o dos profissionais de saúde e os idosos.
A farmacêutica havia apontado, em nota divulgada na segunda-feira (28), que era mais vantajoso manter apenas o trâmite para obtenção do registro definitivo do imunizante, que permite a distribuição do produto em larga escala, inclusive para a rede privada. A Pfizer afirmava que a falta de um contrato definitivo com o governo brasileiro, além de exigências da Anvisa, eram barreiras para acelerar o uso emergencial.
A Anvisa estima que levará até 10 dias para avaliar um pedido de uso emergencial. Não há solicitação deste tipo ainda na agência.
Agora a empresa declara que, “diante dos esclarecimentos feitos pela Agência”, há a possibilidade de a Anvisa “modular pontos específicos do Guia de Submissão para Uso Emergencial, possibilitando uma maior agilidade na submissão desse tipo de processo (uso emergencial)”. A farmacêutica manterá ainda as tratativas para obter o registro definitivo.
O uso da vacina da Pfizer já foi autorizado em mais de 40 países. O Brasil negocia a compra de 70 milhões de doses da vacina, mas o presidente Jair Bolsonaro e o ministro da Saúde, Eduardo Pazuello, têm criticado exigências feitas pela empresa, como cláusula contratual para não responder por eventuais efeitos colaterais do imunizante.
Mesmo sem o contrato fechado, o plano de imunização do Ministério da Saúde prevê que a Pfizer reserve 500 mil doses para o Brasil em janeiro. O documento ainda estima 2 milhões de doses da farmacêutica no primeiro trimestre. A soma até a metade do ano seria de 8,5 milhões de unidades de imunizante. No segundo semestre, cerca de 61 milhões de vacinas chegariam ao país.
A ideia do ministério é usar as doses recebidas no primeiro trimestre para imunizar profissionais de saúde nas capitais e regiões metropolitanas que atuam no combate à Covid-19.
*Estadão
Leia também1 Anvisa e AstraZeneca se reúnem para discutir uso de vacina
2 Aplicação da vacina não excluirá normas de prevenção
3 Demissão de médico gera crise interna no STF e desgasta Fux
4 Covid-19: Anvisa muda regras para uso emergencial de vacinas
5 SP recebe 6° lote da CoronaVac com mais 1,6 milhão de doses